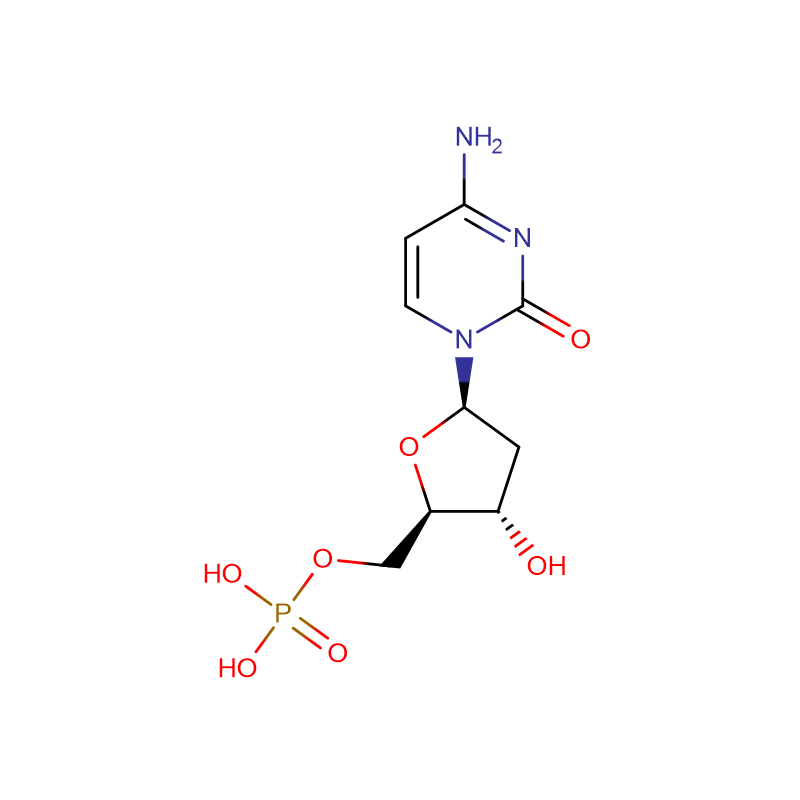
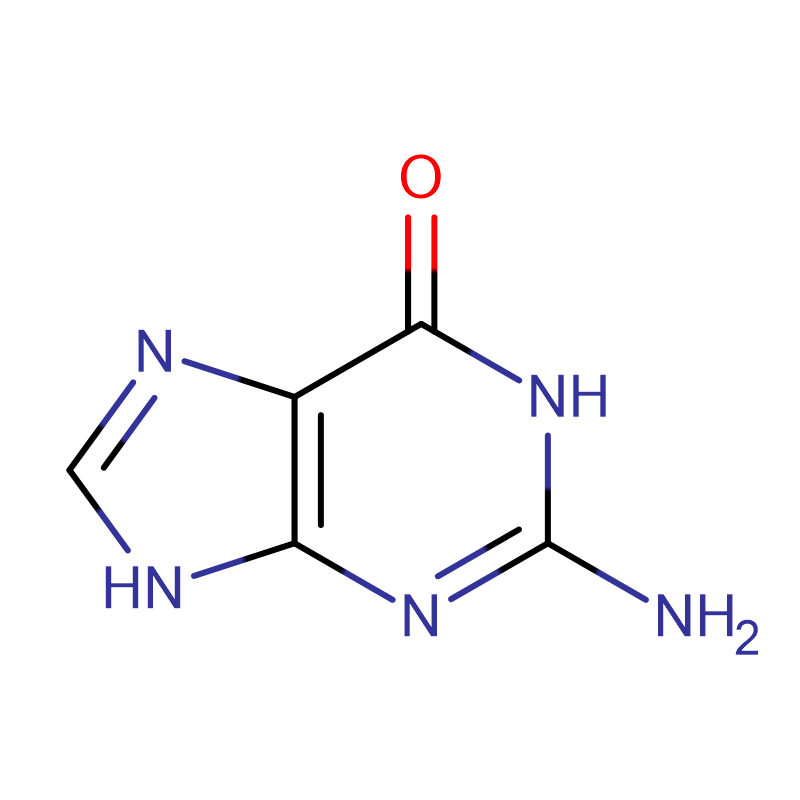
2′-Déoxyuridine Cas:951-78-0
| Numéro de catalogue | XD90583 |
| Nom du produit | 2'-désoxyuridine |
| CAS | 951-78-0 |
| Formule moléculaire | C9H12N2O5 |
| Masse moléculaire | 228,20 |
| Détails de stockage | 2 à 8 °C |
| Code tarifaire harmonisé | 29349990 |
Spécification de produit
| Apparence | Poudre blanche à blanc cassé |
| Essai | 99% |
| Point de fusion | 164 - 168 degrés Celsius |
| Perte au séchage | <1,0 % |
| Résidu à l'allumage | <0,1 % |
L'amélioration de l'utilisation de l'azote chez les bovins est importante pour garantir une production bovine durable.Comme les purines et les pyrimidines (PP) constituent une partie appréciable de l'azote du rumen, une meilleure compréhension de l'absorption et du métabolisme intermédiaire des PP est essentielle.Le présent travail décrit le développement et la validation d'une méthode sensible et spécifique de dosage simultané de 20 purines (adénine, guanine, guanosine, inosine, 2'-désoxyguanosine, 2'-désoxyinosine, xanthine, hypoxanthine), pyrimidines (cytosine, thymine, uracile, cytidine, uridine, thymidine, 2'-désoxyuridine) et leurs produits de dégradation (acide urique, allantoïne, β-alanine, acide β-uréidopropionique, acide β-aminoisobutyrique) dans le plasma sanguin des vaches laitières.La technique basée sur la chromatographie liquide à haute performance couplée à la spectrométrie de masse en tandem à ionisation par électrospray (LC-MS/MS) a été combinée avec des normes d'étalonnage individuelles appariées à la matrice et des composés de référence marqués isotopiquement stables.L'analyse quantitative a été précédée d'une nouvelle procédure de prétraitement consistant en une précipitation à l'éthanol, une filtration, une évaporation et une reconstitution.Les paramètres de séparation et de détection lors de l'analyse LC-MS/MS ont été étudiés.Il a été confirmé que l'utilisation d'un modèle d'étalonnage logarithmique plutôt qu'un modèle d'étalonnage linéaire entraînait un pourcentage de CV inférieur et un test d'absence d'ajustement a démontré une régression linéaire satisfaisante.La méthode couvre des plages de concentration pour chaque métabolite en fonction de celles des échantillons réels, par exemple guanine : 0,10-5,0 μmol/L et allantoïne : 120-500 μmol/L.Le CV % pour les plages de quantification choisies était inférieur à 25 %.La méthode a une bonne répétabilité (CV%≤25%) et une précision intermédiaire (CV%≤25%) et d'excellentes récupérations (91-107%).Tous les métabolites ont démontré une bonne stabilité à long terme et une bonne stabilité intra-série (CV%≤10%).Différents degrés d'effets matriciels absolus ont été observés dans le plasma, l'urine et le lait.La détermination des effets relatifs de matrice a révélé que la méthode convenait à presque tous les métabolites PP examinés dans le plasma prélevé d'une artère et des veines porte hépatique, hépatique et gastrosplénique et, à quelques exceptions près, également pour d'autres espèces telles que le poulet, le porc, vison, humain et rat.