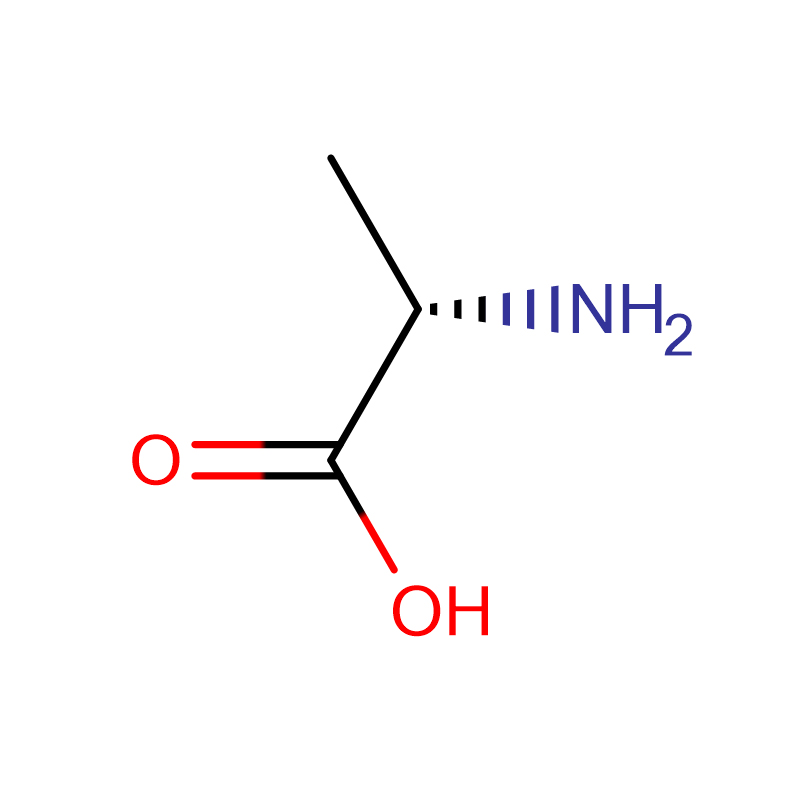
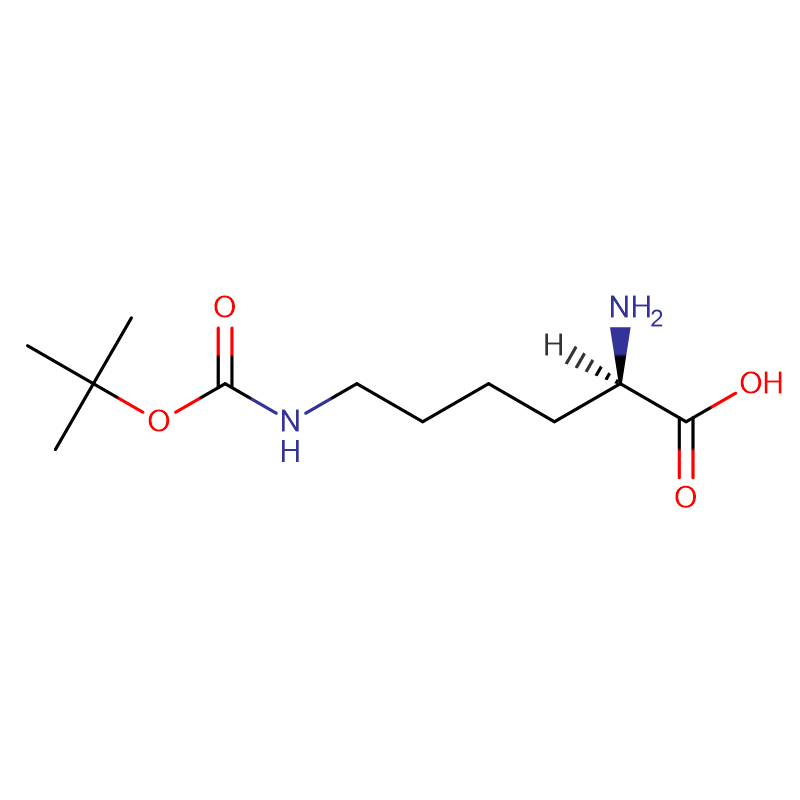
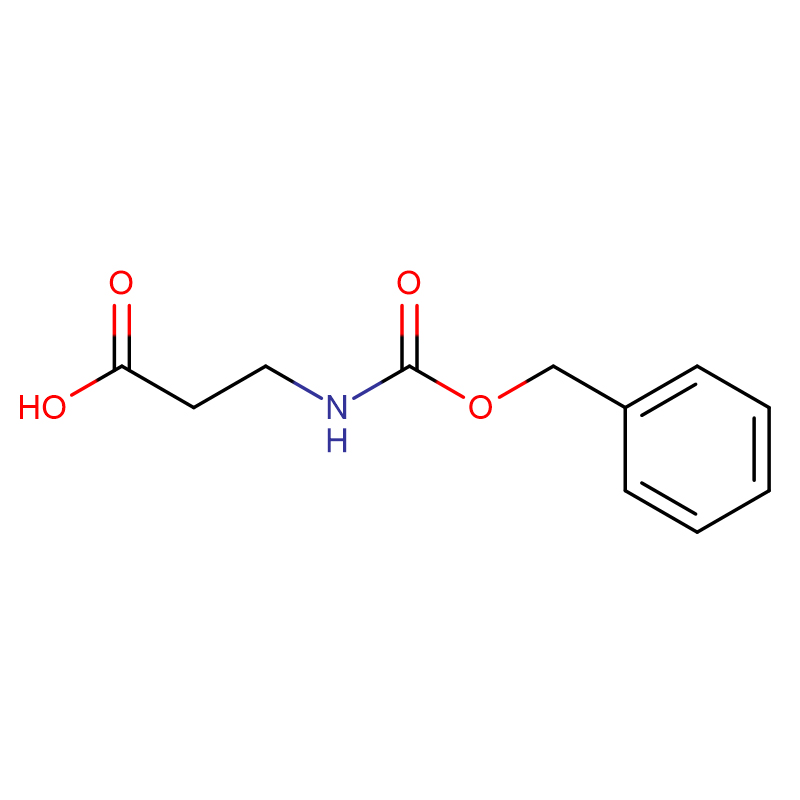
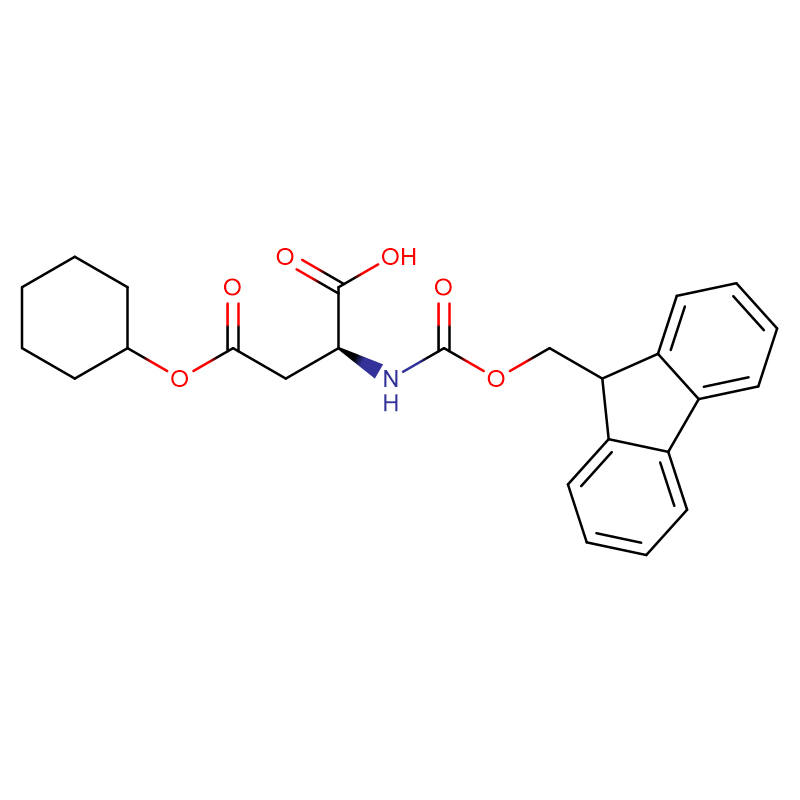
L-Alanine CAS : 56-41-7 99 % de poudre cristalline blanche
| Numéro de catalogue | XD90326 |
| Nom du produit | D-Alanine |
| CAS | 338-69-2 |
| Formule moléculaire | C3H7NO2 |
| Masse moléculaire | 89.09 |
| Détails de stockage | Ambiant |
| Code tarifaire harmonisé | 29224985 |
Spécification de produit
| Apparence | Poudre cristalline blanche |
| Essai | 98,5 - 101,5 % |
| Rotation spécifique | +13,7 à +15,1 |
| Métaux lourds | <0,0015 % |
| pH | 5.5 - 7 |
| SO4 | <0,03 % |
| Perte au séchage | <0,2 % |
| Fer | <0,003 % |
| Résidu à l'allumage | <0,15 % |
| La taille des particules | 200um |
| Cl | <0,05 % |
| Niveau de polluants organiques persistants | Pas de polluants |
Les γ-glutamyltranspeptidases (γ-GT) clivent la liaison γ-glutamyl amide du glutathion et transfèrent le groupe γ-glutamyle libéré dans l'eau (hydrolyse) ou les acides aminés accepteurs (transpeptidation).Ces enzymes omniprésentes jouent un rôle clé dans la biosynthèse et la dégradation du glutathion, ainsi que dans la détoxification des xénobiotiques.Nous rapportons ici la structure cristalline de résolution 3Å de Bacillus licheniformis γ-GT (BlGT) et celle de son complexe avec l-Glu.Les structures aux rayons X confirment que BlGT appartient à la superfamille des hydrolases nucléophiles N-terminales et révèlent que la protéine possède une fente de site actif ouverte similaire à celle rapportée pour l'enzyme homologue de Bacillus subtilis, mais différente de celles observées pour la γ-GT humaine et pour les γ-GT d'autres micro-organismes.Les données suggèrent que la liaison de l-Glu induit une réorganisation de la queue C-terminale de la grande sous-unité BlGT et permet l'identification d'un groupe de résidus acides potentiellement impliqués dans la reconnaissance d'un ion métallique.Le rôle de ces résidus sur la stabilité conformationnelle de BlGT a été étudié en caractérisant l'autotraitement, l'activité enzymatique, la dénaturation chimique et thermique de quatre nouveaux mutants simples Ala.Les résultats montrent que le remplacement de Asp568 par un Ala affecte à la fois l'autotraitement et la stabilité structurelle de la protéine.