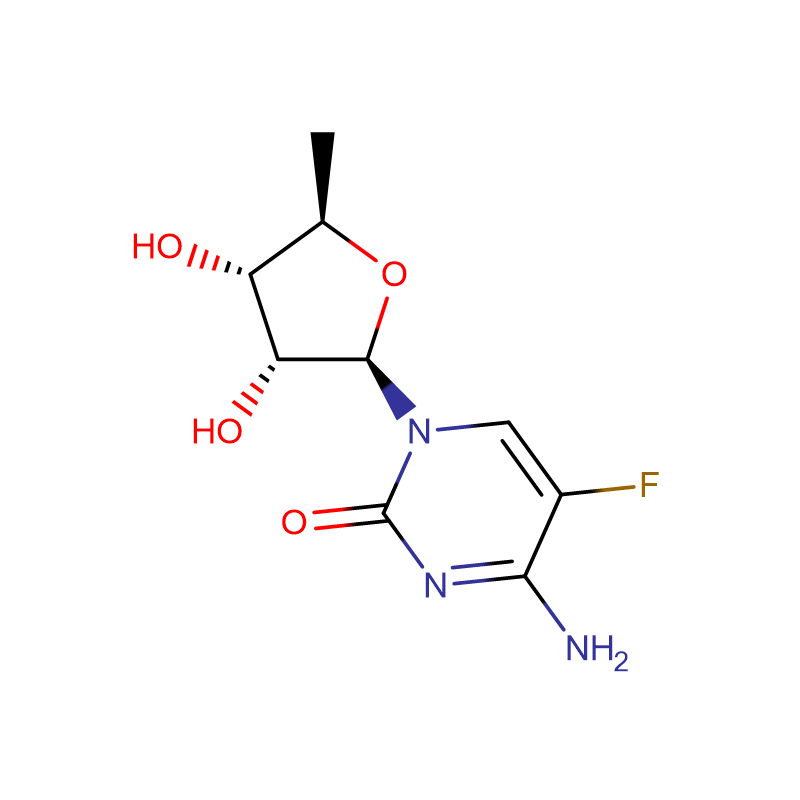
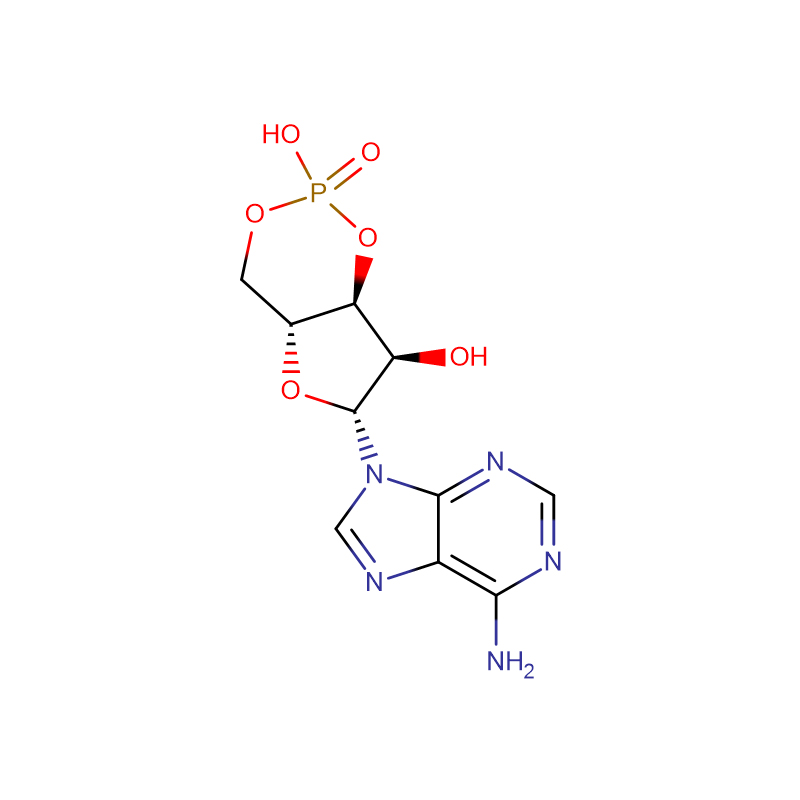
dUMP, sel disodique de 2′-désoxyuridine 5′-monophosphate CAS: 42155-08-8
| Numéro de catalogue | XD90546 |
| Nom du produit | Dump, sel disodique de 2'-désoxyuridine 5'-monophosphate |
| CAS | 42155-08-8 |
| Formule moléculaire | C9H11N2Na2O8P |
| Masse moléculaire | 352.15 |
| Détails de stockage | 2 à 8 °C |
| Code tarifaire harmonisé | 29349990 |
Spécification de produit
| Essai | 99% |
Pour quantifier spécifiquement plusieurs métabolites du 5-fluorouracile (5-FU) et deux nucléotides monophosphates endogènes, nous avons développé une méthode originale basée sur une chromatographie liquide-spectrométrie de masse en tandem (LC-MS/MS).Ce test a permis de déterminer : (i) la production intracellulaire de 5-fluoro-2′-désoxyuridine-5′-monophosphate (5-FdUMP) à partir de 5-FU ou de 5-fluoro-2′-désoxyuridine (5-FdUrd) , (ii) l'impact de la concentration de 5-FdUMP sur le rapport intracellulaire 2′-désoxyuridine-5′-monophosphate (dUMP)/thymidine-5′-monophosphate (TMP), et (iii) l'étendue de la sécrétion de 5-FdUMP et 5-FU de cellules humaines cultivées par des transporteurs ABC.Dans nos conditions expérimentales, les cellules ont été incubées avec du 5-FU ou du 5-FUrd.Ensuite, les protéines cellulaires ont été précipitées par du méthanol.Cette procédure a fourni une récupération d'extraction élevée.De plus, pour mesurer la sécrétion de 5-FU et 5-FdUMP à partir des cellules, nous avons effectué une quantification de ces molécules en milieu de culture.Les milieux ont été injectés directement (5-FU) ou ont subi une extraction en phase solide à l'aide d'une cartouche d'extraction Oasis Wax (5-FdUMP).La séparation des analytes a été réalisée sur une colonne dC18 Atlantis 3,5 μm (100 mm × 2,1 mm id) en mode isocratique en utilisant un tampon formiate d'ammonium/méthanol/eau (5/5/90, v/v) comme phase mobile.Le temps d'exécution n'a pas dépassé 6,2 min.Les analytes ont été ionisés dans une interface électrospray en mode ions négatifs.Nous avons validé la méthode sur une plage de 2,5 à 150 ng mL −1 selon les composés.La variabilité intra- et inter-essai était inférieure à 10 % sur sept jours.Tous les composés étaient stables dans les cellules ou dans le milieu de culture lorsque les échantillons étaient stockés à -20 ° C pendant au moins deux semaines et après trois cycles de congélation-décongélation.Aucun effet de matrice n'a été observé dans les deux milieux.