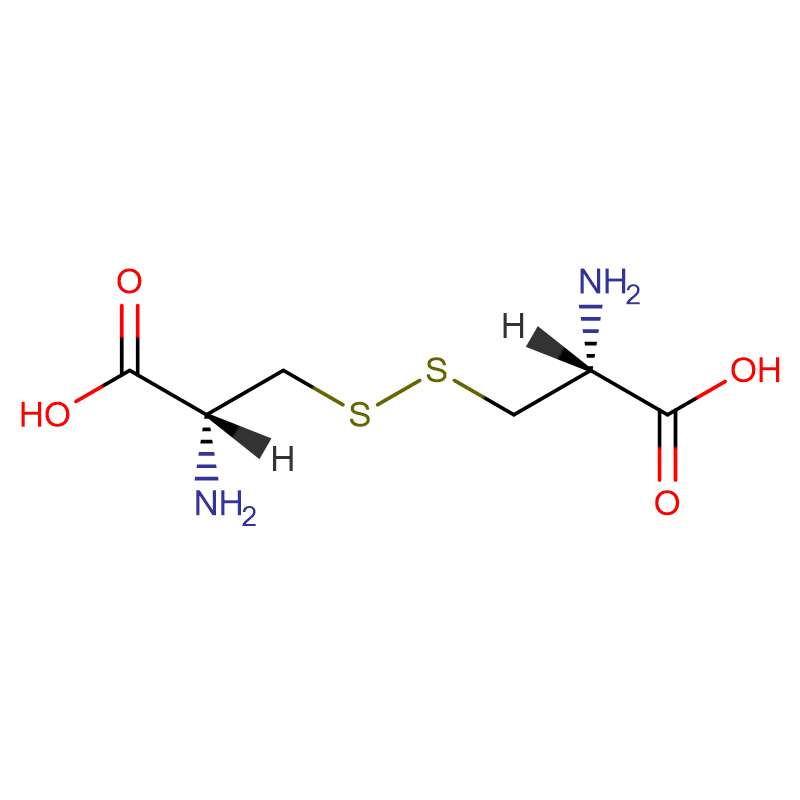
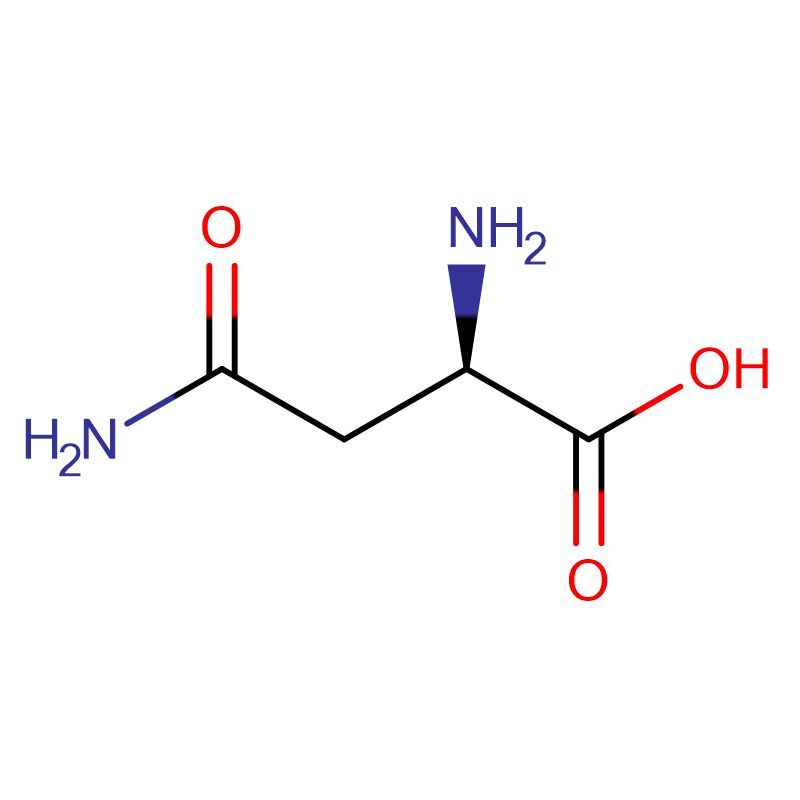
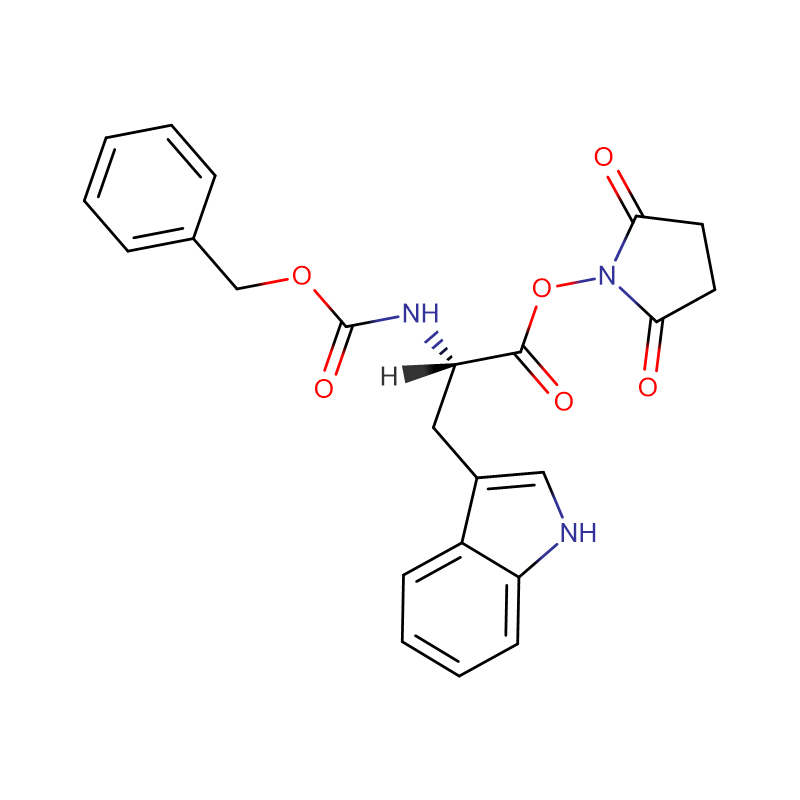
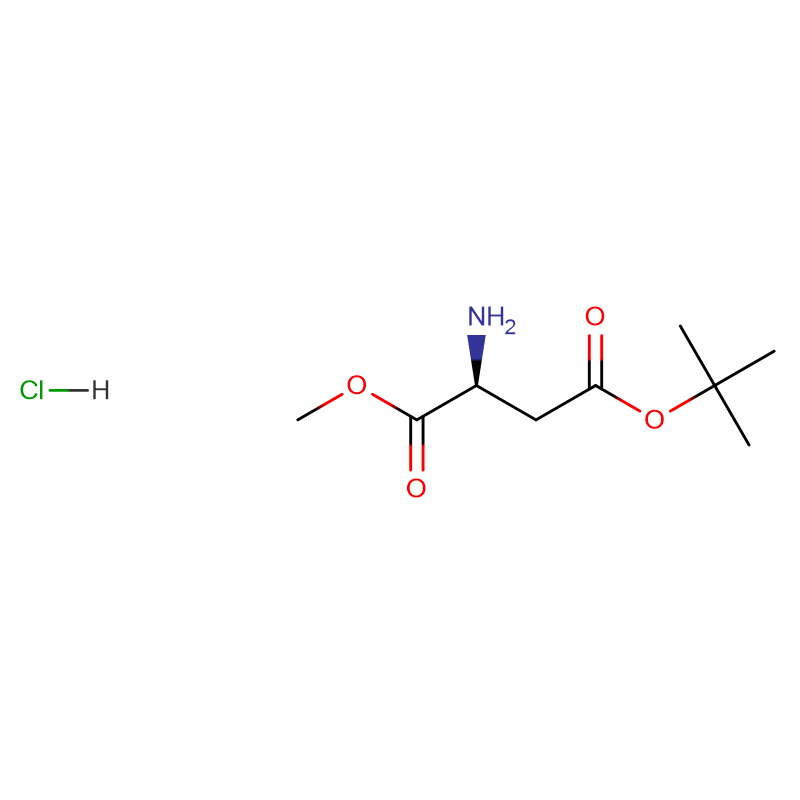
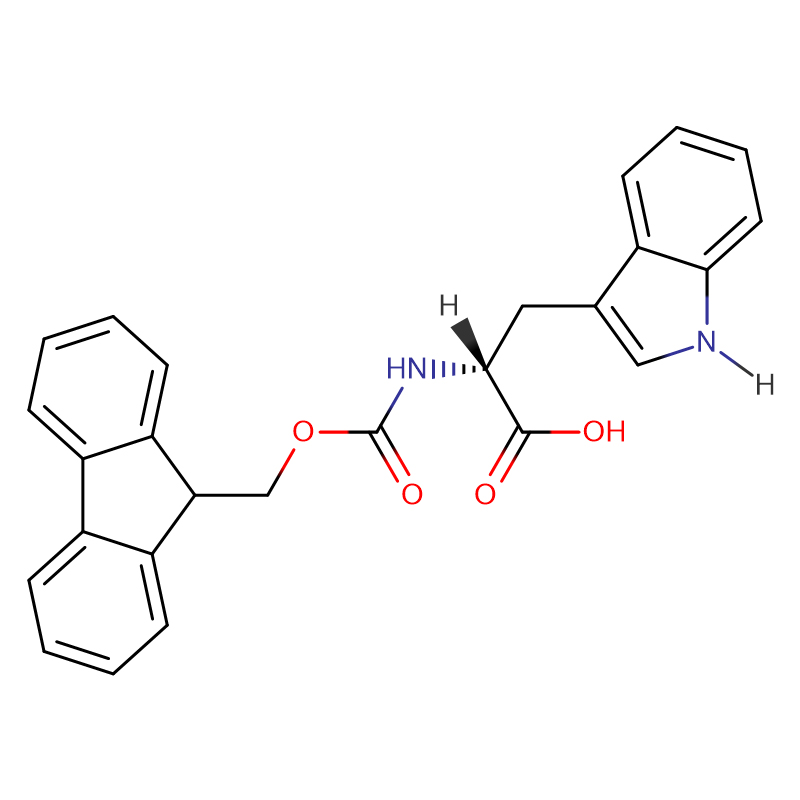
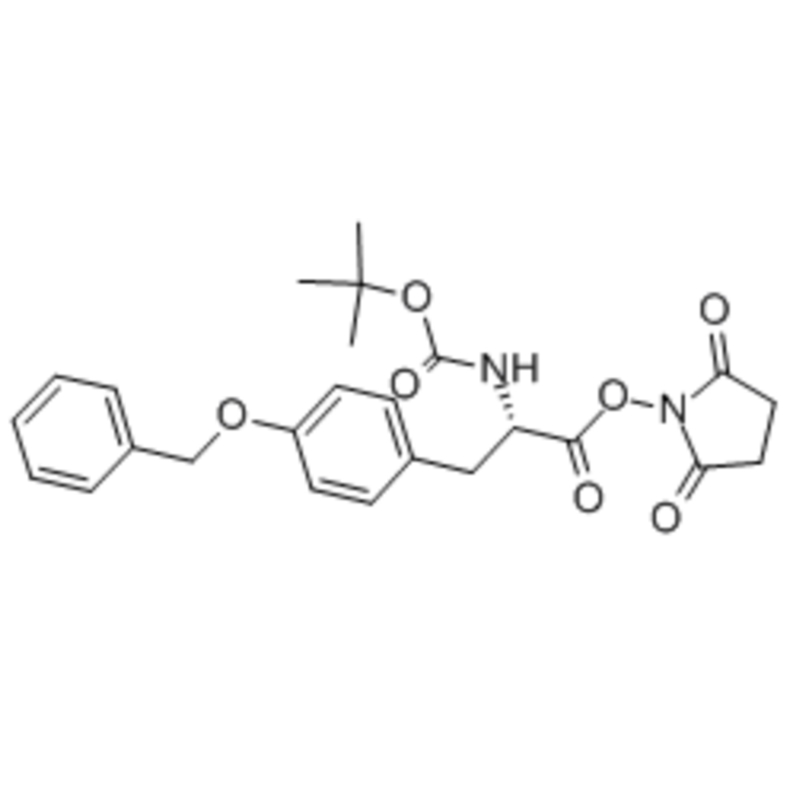
L-Cystine CAS : 56-89-3 99 % de cristaux blancs ou de poudre cristalline
| Numéro de catalogue | XD90322 |
| Nom du produit | L-Cystine |
| CAS | 56-89-3 |
| Formule moléculaire | C6H12N2O4S2 |
| Masse moléculaire | 240,30 |
| Détails de stockage | Ambiant |
| Code tarifaire harmonisé | 29309013 |
Spécification de produit
| Apparence | Cristaux blancs ou poudre cristalline |
| Essai | 99% |
| Grade | USP32 |
| Rotation spécifique | -215° à -225° |
| Métaux lourds | <0,0015 % |
| AS | 1,5 ppm maximum |
| SO4 | 0,040 % maximum |
| Fe | <0,003 % |
| Perte au séchage | 0,20 % maximum |
| Résiduel à l'allumage | 0,10 % maximum |
| Cl | 0,10 % maximum |
Les structures cristallines des complexes de carboxypeptidase T (CpT) avec des analogues de substrat de phénylalanine et d'arginine - acide benzylsuccinique et acide (2-guanidinoéthylmercapto)succinique - ont été déterminées par la méthode de remplacement moléculaire à des résolutions de 1,57 Å et 1,62 Å pour clarifier le large profil de spécificité de substrat de l'enzyme.Les résidus conservateurs Leu211 et Leu254 (également présents dans la carboxypeptidase A et la carboxypeptidase B) se sont révélés être des déterminants structuraux pour la reconnaissance des substrats hydrophobes, alors que Asp263 était pour la reconnaissance des substrats chargés positivement.Des mutations de ces déterminants modifient le profil du substrat : le variant CpT Leu211Gln acquiert des propriétés de type carboxypeptidase B, et le variant CpT Asp263Asn la sélectivité de type carboxypeptidase A.La boucle Pro248-Asp258 interagissant avec Leu254 et Tyr255 s'est avérée responsable de la reconnaissance du résidu C-terminal du substrat.La liaison au substrat au niveau du sous-site S1' conduit au déplacement dépendant du ligand de cette boucle, et le mouvement de la chaîne latérale Leu254 induit le réarrangement de la conformation du résidu Glu277 crucial pour la catalyse.Il s'agit d'un nouvel aperçu de la sélectivité du substrat des métallocarboxypeptidases qui démontre l'importance des interactions entre le sous-site S1' et le centre catalytique.